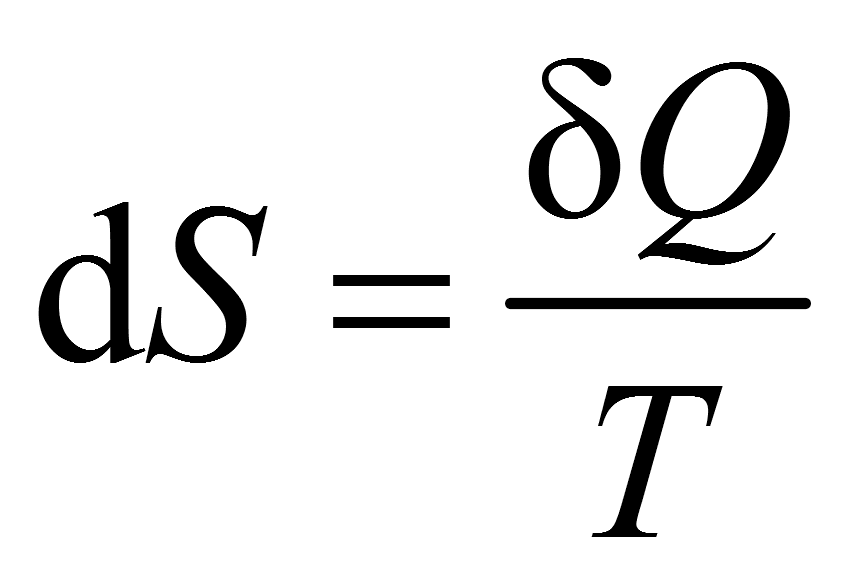
Berechnung der Entropieänderung
a) Wie ist die Entropie definiert und welche Bedeutung hat sie?
b) Wie groß ist die Entropieänderung bei Mischung von 40 Liter Wasser der Temperatur 80 Grad C mit 60 Liter Wasser der Temperatur 15 Grad?
c = 4,19 kJ/ (kg K)
Lösung
a) Wie ist die Entropie definiert und welche Bedeutung hat sie?
Die Entropie ist eine Größe, die benötigt wird, um die Arbeitsfähigkeit der Energie zu beschreiben, da die Energiemenge alleine nichts über die Arbeitsfähigkeit aussagt. Es können nur Änderungen der Entropie erfasst werden. Man nennt Zustandsänderungen mit konstanter Entropie auch isentrop.
Entropie
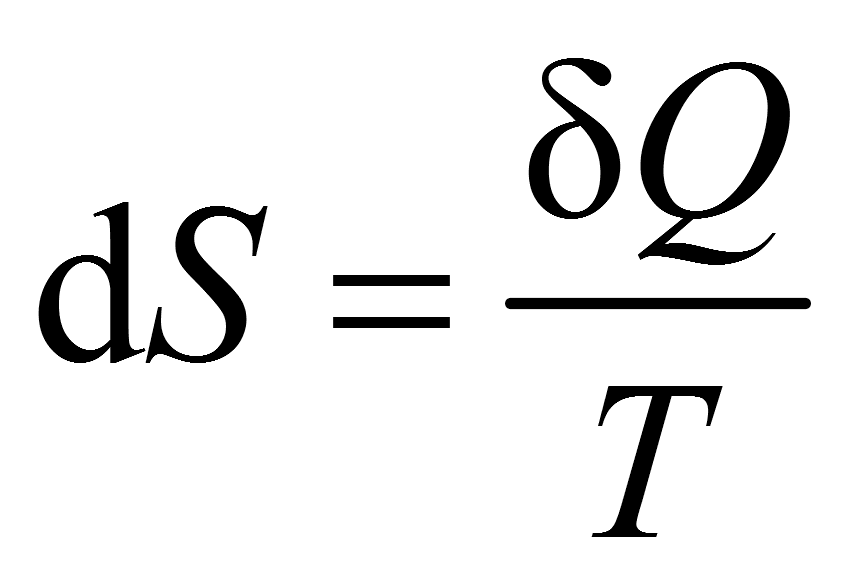
Die Entropieänderung ist bei Wärmezufuhr positiv, bei Wärmeabfuhr negativ.
b) Wie groß ist die Entropieänderung bei Mischung von 40 Liter Wasser der Temperatur 80 Grad C mit 60 Liter Wasser der Temperatur 15 Grad?
Es muss die Richmannsche Mischungsregel angewendet werden, um die Temperatur des Gemisches der beiden Flüssigkeit zu ermitteln. Die Mischungsregel ist eine Regel zur Bestimmung der Mischungstemperatur, die sich beim Zusammenbringen zweier (oder mehrerer) Körper/ Flüssigkeiten unterschiedlicher Temperatur einstellt. Die Wärmemenge der Komponenten ist gleich der Wärmemenge der Mischung:
(c1 · m1 · T1 + c2 · m2 · T2) = Tm · (c1 · m1 + c2 · m2)
Hier ist c1 = c2
(m1 · T1 + m2 · T2) = Tm · (m1 + m2)
T1 = 273 + 80 = 353 K
T2 = 273 + 15 = 288 K
(40 · 353 + 60 · 288) = Tm · (40 + 60)
Tm = 314 K
Die gesamte Änderung der Entropie setzt sich aus der Änderung der Entropien der einzelnen Systeme zusammen.
Vereinbart werden die Dimensionen: kg, K, kJ
ΔS1 = c · m1 · ln (Tm/ T1)
ΔS2 = c · m2 · ln (Tm/ T2)
ΔS1 = 4,19 · 40 · ln (314 / 353)= -19,6212 kJ/K
ΔS2 = 4,19 · 60 · ln (314 / 288)= 21,7291 kJ/K
ΔS1 + ΔS2 = -19,6212 + 21,7291 = 2,1079 kJ/K
Die Entropieänderung ist positiv.